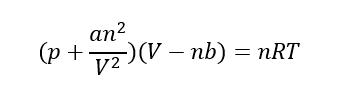理想气体状态方程
理想气体状态方程
一、理想气体
理想气体是指一种理想化模型气体,其分子具有如下特征:
分子之间不存在相互作用力
分子本身的体积可以忽略不计
在任意温度和压力下都满足以下气体实验定律
Boyle 玻意耳定律(等温变化):
p_1 V_1=p_2 V_2
Charles查理定律(等容变化)
p_1/T_1=p_2/T_2
Gay Lussac 盖-吕萨克定律(等压变化)
V_1/T_1=V_2/T_2
二、理想气体状态方程
理想气体状态方程仅适用于接近大气压的压力。表示一定质量(亦即一定物质的量)的某种理想气体,在从状态1变化到状态2时压强p跟体积V的乘积与热力学温度T的比值保持不变,表达为:
p_1 V_1/T_1=p_2 V_2/T_2 "或:" pV/T=const
将此方程结合Avogadro 阿伏伽德罗定律V/n=const,得到:
pV=nRT
其中
p压力 pressure (psia);
V体积 volume (cu.ft);
N物质的量 the number of lb. moles, where one Ib. mole
is the molecular weight of then=gas expressed in pounds.
R气体常数 the universal gas constant which, for the above units,
has the value10.732 psia.cu.ft/lb. mole.°R.
T热力学温度absolute temperature - degrees Rankine (°R=460+°F)
三、真实气体状态方程
实际气体与理想气体的偏差
在高压、低温等极端条件下,实际气体不等于理想气体。其主要原因为:
分子间存在引力
分子体积不可忽略
为了修正理想气体模型,引入范德华方程/凡德瓦耳方程(van der Waals equation):
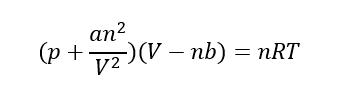
其中
a表示分子间吸引力 Inter molecular attractive force
b表示气体分子占据体积 Volume occupied by one mole of the gas
四、总结
理想气体状态方程是气体热力学的基础模型,其核心意义在于:
• 建立了压力、体积、温度之间的定量关系
• 是工程计算(如油气开发、流体模拟)的基础
• 在常规条件下具有良好的适用性
• 在应用条件下需使用修正模型(如范德华方程)